NEWS24.CO.ID - Kemajuan teknologi rekayasa genetik mencapai puncaknya setelah ditemukan teknologi peng-edit-an DNA melalui teknologi CRISPR (interspaced short palindromic repeat).
Demikian pula aplikasi pemanfaatan gen vektor virus yang bisa diaplikan langsung ke tubuh pasien (in vivo), atau sel yang diambil dari pasien yang dimodifikasi di laboratorium (ex vivo) dan kemudian dimasukkan kembali ke dalam tubuh.
Perkembangan teknologi pengeditan DNA telah memicu kegembiraan atas terapi genetik dan merupakan area perkembangan yang sangat penting.
Ada Tiga teknologi pengeditan gen utama dikelompokkan secara berurutan; “interspaced short palindromic repeat (CRISPR), Cas-associated nucleases, programmable nucleases”, seperti: zinc-finger nucleases (ZFNs) dan transcription activator-like effector nucleases (TALENs).
Aplikasi klinis pertama adalah CRISPR/Cas9 digunakan untuk seseorang dengan mutasi pada gen CEP290 yang menyebabkan degenerasi retina.
Uji klinis juga sedang dilakukan untuk mengevaluasi pendekatan terapeutik ini untuk pengobatan kanker dan penyakit sel sabit.
Demikian pula studi pertama CRISPR/Cas9 sebagai terapi potensial untuk CF menggunakan knock-in spesifik lokasi dari urutan CFTR yang benar untuk mengembalikan fungsi CFTR dengan kekuatan terdapat dalam organoid sel induk usus manusia yang berasal dari pasien homozigot untuk mutasi.
Bahkan tim peneliti dan penemu CRISPR/Cas9 telah dinobatkan sebagai penerima penghargaan prestisius Nobel Prize kepada Jennifer Doudna & Emmanuelle Charpentier, dari Universitas California, Berkeley pada tahun 2020.
Baca juga: Prinsip Dasar Farmakologi Sel dan Genetik
Efektivitas CAR-T Cell pada Glioblastoma
Glioblastoma merupakan penyakit kanker pada manusia yang paling mematikan, dengan tingkat harapan hidup yang sangat rendah, meskipun telah dilakukan operasi, pengobatan radiasi, dan kemoterapi.
Pengobatan tumor otak Glioblastoma selama ini mengalami kesulitan dan keterbatasan karena beberapa mekanisme resistensi: kertebatasan masuknya obat ke dalam kompartemen sistem saraf pusat oleh penghalang sawar darah-otak; penangkal obat untuk sampai ke sasaran tumor; heterogenitas yang luas pada glioblastoma berkontribusi terhadap resistensi terapeutik yang signifikan dengan mencegah kontrol yang memadai dari seluruh massa tumor, dengan obat tunggal dan dengan memfasilitasi mekanisme pelepasan dari agen yang ditargetkan.
Karakteristik glioblastoma yang mirip sel punca meningkatkan resistensi terhadap kemoterapi, radiasi, dan imunoterapi melalui peningkatan regulasi transporter akhir, promosi proliferasi sel punca glioblastoma, dan penekanan immunologik.
Bahkan teknik molekuler sedang dikembangkan untuk menargetkan tumor secara spesifik, sehingga akan meningkatkan efektivitas atau kemanjuran pengobatan dan kesembuhan penderita glioblastoma.
Dengan menggunakan teknologi berbasis farmakologi sel dan genetik, berupa onko immune vaksinomik, menjadi solusi yang terbaik.
Berdasarkan hasil uji klinis, fase 1, 2, 3 dari metode dendritic vaccine ditemukan hasil yang menakjubkan, sebagai berikut:
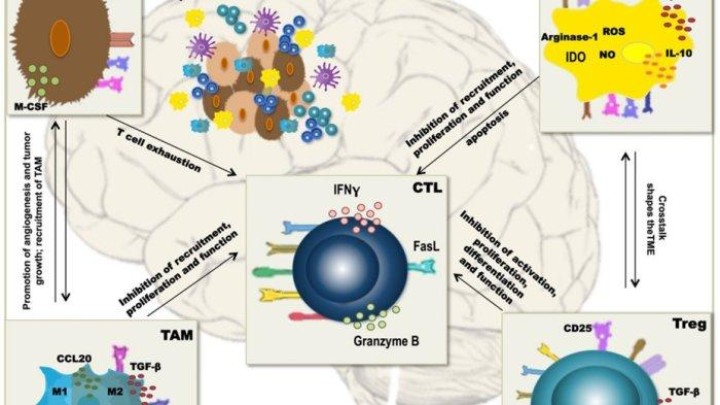
Dalam GBM, makrofag terkait tumor (TAM), sel penekan turunan myeloid (MDSC), dan sel T regulator (Treg) membentuk lingkungan mikro tumor imunosupresif yang kuat (TME), yang menghambat imunitas antitumor dan dengan demikian mengganggu dendritik vaksinasi sel (DCV).
Selain mekanisme pelepasan imun intrinsik dari sel tumor, molekul pos pemeriksaan imun, seperti PD-L1, PD-L2, Tim-3, Lag-3, CD155, dan galektin-9 yang biasanya mengontrol tingkat respons imun, diekspresikan pada sel imunosupresif TME, berkontribusi terhadap disfungsi sel-T dan selanjutnya respon imun antitumor yang tidak efisien.
Sel TME mengeluarkan sitokin seperti TGF-b, IL-10, dan IL-35 dan kemokin CCL20, CCL22, dan CXCL12, yang menghambat proliferasi dan fungsi sel-T dan berkontribusi pada crosstalk antara berbagai jenis sel TME, sehingga semakin meningkatkan imunosupresi.
Mekanisme tambahan meliputi aktivitas indoleamin-2,3-dioksigenase (IDO) dan arginase-1 serta produksi oksigen reaktif spesies (ROS) dan oksida nitrat (NO), semuanya mengganggu diferensiasi, ekspansi, dan fungsi sel T efektor yang tepat.
UJI KLINIS FASE I/II: Pada uji klinis fase I/II dari tim kami di Aivita Biomedical California, dengan menggunakan metode multi-center, yang bertujuan untuk melihat tingkat kelangsungan hidup pasien Glioblastoma, dengan masa penilaian 15 bulan setelah pendaftaran penggunaan Vaksin Dendritik dibangdingkan dengan standard.
Dalam penelitian tersebut, Kriteria inklusif yang digunakan secara ketat, berupa: (1) diagnosis GBM primer, (2) usia <70 tahun pada saat reseksi tumor, (3) kultur sel GBM, (4) pengumpulan monosit dengan leukapheresis, (5) Status Kinerja Karnofsky (KPS) > 70 setelah pemulihan bedah.
Sel dendritik (DCs) dibedakan dari monosit autolog, kemudian diinkubasi dengan antigen tumor autolog (ATA) dari lisat garis sel GBM untuk menghasilkan setiap vaksin DC-ATA khusus pasien.
Selanjutnya, pasien diberikan dosis 500 mcg granulocyte-macrophage colony-stimulating factor (GM-CSF) pada saat injeksi subkutan pada minggu ke 1, 2, 3, 8, 12, 16, 20 dan 24.
Pasien didaftarkan sesaat sebelum memulai standar temozolomide (TMZ) bersamaan dan terapi radiasi (RT) untuk perawatan intensif setelah pemulihan dari RT/TMZ.
Tingkat keberhasilan Cell Lines adalah 71/73 (97 persen); tingkat keberhasilan monosit adalah 63/65 (97 persen). KPS = rata-rata 83,2.
Tidak ada pasien yang mengalami toksisitas atau keracunan.
Baca juga: Masa Depan Teknologi Farmakologi Terapi Sel dan Genetik
Kesimpulan dari Uji Klinis Fase I/II adalah: Terdeteksi MGMT promoter methylation pada 21 orang pasien (35 persen), juga terdeksi mutated IDH pada 7 orang pasien (12%), dan terdapat keduanya pada 25 orang pasien (42%).
Terdapat peningkatan harapan hidup 14.7 bulan, bahkan 18 bulan pada Overall Survival rates adalah 59% vs. 35% MGMT promotor methylation, 71% vs 40% untuk IDH mutation, 58% vs 32% bagi lainnya.
Sehingga menunjukkan hasil yang sangat signifikan, yang berarti terjadi peningkatan survival rate atau angka harapan hidup yang signifikan pada pasien GBM primer yang diobati dengan AV-GBM-1.
Dalam, UJI KLINIS FASE III: yang bertujuan mengobati Glioblastoma, penyakit yang sangat berat dan merupakan penyebab kematian primer (the most lethal primary brain cancer).
Bahan yang menjadi obyek penelitian fase tiga ini adalah autologous tumor lysate-loaded dendritic cell vaccine (DCVax-L) dibandingkan dengan pengobatan standard of care (SOC) Glioblastoma, dalam memperpanjang angka harapan hidup (survival among patients) pada pasien glioblastoma.
Uji Klinis fase 3 ini, bersifat: prospektif, externally controlled nonrandomized trial dibandingkan dengan overall survival (OS) pada pasien-pasien yang baru terdiagnosis “newly diagnosed glioblastoma (nGBM)” dan pasien pasien rekuren “recurrent glioblastoma (rGBM)” yang diobati dengan DCVax-L plus SOC vs. standar SOC sebagai Kontrol.
Uji Klinis ini bersifat internasional, multi senter yang dilaksanakan di 94 senter penelitian dari 4 negara didunia, dan berlangsung dari Agustus 2007 s/d September 2021.
Pelaksanaan uji klinis fase 3 ini, berlangsung dengan pemberian DCVax-L plus SOC temozolomide.
Untuk kasus baru nGBM dibandingkan dengan kontrol yaitu pasien yang menerima SOC temozolomide dan placebo; Demikian juga dengan kasus rekuren (rGBM) mendapatkan obat standar yang telah disetujui untuk rGBM.
Berdasarkan data akhir primer dan sekunder dibandingkan hasil akhir dari semua overall survival (OS) gabungan nGBM and rGBM, demikian pula dibandingkan secara konprehensip sesuai populasi dan secara ramdom uji klinis fase 3, didapatkan hasil sebagai berikut: Total 331 pasien yang mengikuti uji klinis, dengan 232 pasien mendapatkan DCVax-L dibandingkan 99 pasien merupakan placebo group, Hasilnya berupa: Median OS (mOS) untuk 232 pasien yang nGBM menerima DCVax-L sebesar 19.3 (95% CI, 17.5-21.3) bulan, dan (22.4 months from surgery) vs 16.5 (95% CI, 16.0-17.5) bulan untuk kontrol pasien (HR = 0.80; 98% CI, 0.00-0.94; P = .002).
Survival 48 bulan 15.7% vs 9.9%, dan 60 bulan, sehingga 13.0% vs 5.7%.
Ada 64 pasien dengan rGBM menerima DCVax-L, mOS adalah 13.2 (95% CI, 9.7-16.8) dari yang mengalami relapse vs 7.8 (95% CI, 7.2-8.2) bulan disbanding control (HR, 0.58; 98% CI, 0.00-0.76; P < .001).
Survival pada 24 dan 30 bulan setelah mengalami rekuren adalah 20.7% vs 9.6% dan 11.1% vs 5.1%, secara berurutan.
Berdasarkan data diatas, terjadi peningkatan perpanjangan usia dan harapan hidup pada pasien nGBM yang menerima methylated MGMT & DCVax-L disbanding dengan kontrol (HR, 0.74; 98% CI, 0.55-1.00; P = .03).
Baca juga: Rahang Bawah yang Kurang Berkembang Bisa Menyebabkan Seseorang Ngorok Ketika Tidur
Pada penelitian ini penambahan Vaksin Dendritik (DCVax-L) ke pasien GBM dalam ukuran Survival Overall Care (SOC) mengalami peningkatan dan perbaikan klinik yang sangat signifikan dan berarti dalam memperpanjang usia harapan hidup pada kedua jenis pasien nGBM & rGBM dibandingkan dengan pengobatan kontenporer atau pengobatan standar selama ini.
Kesimpulan: Pada Uji Klinis Fase III ini, faktanya pemberian DCVax-L dibandingkan dengan pengobatan standard SOC, memperlihatkan hasil yang sangat berarti secara statistik dengan gambaran perpanjangan angka harapan hidup (overall survival) pada penderita Glioblastoma disbanding control (Hasil ini ditemukan pada kedua group nGBM dan rGBM).
Bahkan pemberian DCVax-L memperlihatkan hasil yang sangat aman, yang terlihat pada kurva diatas.
Baca juga: Faktor Genetik adalah Salah Satu Faktor Risiko Kanker Payudara, Simak Ulasan dr. Sumadi Lukman Anwar
Dikutip dari pidato pengukuhan Guru Besar Prof. dr. Taruna Ikrar, M. Biomed., Ph.D. di Fakultas Kedokteran, Universitas Malahayati, Lampung dengan Judul ERA BARU PENGOBATAN KANKER DAN PENYAKIT DEGENERATIF, BERBASIS FARMAKOLOGI SEL DAN GENETIK: FOKUS STUDI EFEKTIVITAS VAKSIN DENDRITIK CAR-T (Chimeric Antigen Receptor T-Cell) PADA KASUS GLIOBLASTOMA.
(Tribunhealth.com/DN)
Baca berita lain tentang kesehatan di sini.
Sumber : TRIBUNNEWS.COM
 Monday, Jun 10, 2024 | 12:00 pm LT
Monday, Jun 10, 2024 | 12:00 pm LT Monday, Jun 10, 2024 | 12:00 pm LT
Monday, Jun 10, 2024 | 12:00 pm LT Monday, Jun 10, 2024 | 12:00 pm LT
Monday, Jun 10, 2024 | 12:00 pm LT Monday, Jun 10, 2024 | 12:00 pm LT
Monday, Jun 10, 2024 | 12:00 pm LT Monday, Jun 10, 2024 | 12:00 pm LT
Monday, Jun 10, 2024 | 12:00 pm LT Monday, Jun 10, 2024 | 12:00 pm LT
Monday, Jun 10, 2024 | 12:00 pm LT